ErythroMer: гонка за идеальным заменителем крови – от коровьего молока до наших дней
Является ли имитация клеток ключом к созданию универсальной помощи от кровотечения?

Теодор Гайярд Томас и эксперимент с молоком
В Нью-Йорке в XIX веке Теодор Гайярд Томас был известным гинекологом. Причиной, как ни странно, было молоко. Между 1873 и 1880 годами смелая идея переливания молока в качестве заменителя крови тестировалась по всем Соединенным Штатам. Томас был самым ярым сторонником такой практики.
В то время сильное кровотечение часто было смертным приговором. Переливание крови практиковалось, но это было своего рода лотереей. Медицинская наука все еще находилась на расстоянии 30 лет от открытия групп крови. Пациенты, которым переливали несовместимую кровь, страдали от обесцвечивания мочи, зуда и иногда фатального осложнения: гемолитического шока, при котором их собственная иммунная система атаковала перелитые клетки.
Врачи в США искали что-то менее рискованное, чтобы стабилизировать кровоточащую пациентку. Томас был уверен, что решением будет молоко. В 1875 году Томас ввел 175 миллилитров коровьего молока женщине с сильным маточным кровотечением после операции по удалению раковых яичников. Сначала пациентка «жаловалась, что ее голова вот-вот лопнет». Вскоре у нее поднялась высокая температура и необычно высокая частота сердечных сокращений, но через неделю она выздоровела. Впоследствии Томас провел 7 отдельных переливаний молока, опубликовав свои результаты в нескольких медицинских журналах и предсказал их «блестящее и полезное будущее».
Кролик как начало новой эпохи в медицине
Ожидаемого будущего не произошло: в следующем десятилетии были введены солевые растворы, которые используются и по сей день, как гораздо менее опасная, но временная мера для экстренной остановки кровотечения.
Однако потребность в заменителях крови сохраняется. И в прошлом году в лаборатории в Балтиморе был проведен опыт. У кролика откачали часть крови и заменили её экспериментальным заменителем крови под названием ErythroMer. Благодаря ErythroMer переливание крови кролика прошло успешно. Частота сердечных сокращений и артериальное давление животного стабилизировались.
Разработанный врачом Алланом Доктором и его коллегами, ErythroMer сделан из «переработанного» человеческого гемоглобина (белок в эритроцитах, который переносит кислород из легких по всему телу), обернутого в мембрану, имитирующую клетку. Доктор является ярым сторонником переносчиков кислорода на основе гемоглобина (hemoglobin-based oxygen carriers, HBOC), таких как ErythroMer и его предшественники.
Решение проблемы сроков годности донорской крови
Срок годности донорской крови составляет всего 42 дня. Ее также недостаточно, даже в развитых странах с хорошо организованными системами донорства крови: в январе 2022 года организация Американский Красный Крест, которая распределяет 40% донорской крови США, объявила о первом в истории национальном кризисе крови. Кризис связан с тем, что запасы крови — особенно драгоценной и универсальной О отрицательной (I -), — упали на опасный уровень. Между тем, геморрагический шок, вызванный тяжелой потерей крови, ежегодно убивает около 2 миллионов человек во всем мире.
Искусственная кровь, возможно, могла бы заполнить эту пустоту. В условиях, где трудно достать свежую кровь, например, на фронте и в сельской местности, ErythroMer можно вводить на месте, чтобы поддерживать необходимый приток кислорода к органам до тех пор, пока человек не будет доставлен в больницу.
ErythroMer – это сублимированный порошок, который можно использовать в течение многих лет, и его можно восстановить, просто смешав с широкодоступным физиологическим раствором. ErythroMer должен быть безопасен для любой группы крови, потому что его мембрана не содержит поверхностных белков эритроцитов, которые вызывают несовместимость.
Лучше, чем природа
Десятилетия усилий не привели к разработке хорошего заменителя эритроцитов, переносящих кислород. Новый кандидат, ErythroMer, все еще проходит доклинические испытания, но может оказаться более долговечным и универсальным, чем настоящий препарат.
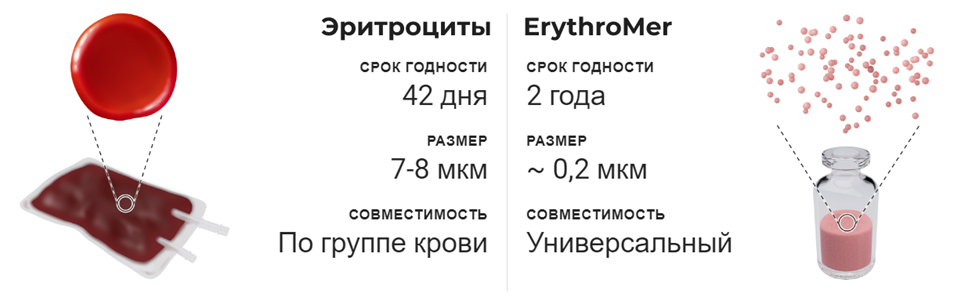
Сравнение эритроцитов и ErythroMer
На данный момент в США коммерчески недоступен заменитель человеческой крови. Поэтому у нас нет доступа к крови для людей, умирающих от потери крови вне больницы, как отметил Доктор. Доктор является соучредителем и главным научным сотрудником KaloCyte, компании, которая надеется превратить ErythroMer в коммерческий продукт.
В прошлом году Агентство перспективных оборонных исследовательских проектов (DARPA) объявило о выделении гранта в размере 46 миллионов долларов консорциуму под руководством UMD на разработку долгосрочного заменителя крови, пригодного для использования в полевых условиях, в основе которого лежит ErythroMer.
«ErythroMer примечателен своей детальной имитацией функции естественных эритроцитов», — говорит Жан-Поль Кретьен, менеджер программы в Управлении биологических технологий DARPA и бывший военнослужащий военно-морского флота.
Карина Язданбахш, вице-президент и директор по исследованиям New York Blood Center Enterprises, соглашается, называя ErythroMer «многообещающим» для использования при травмах и других чрезвычайных ситуациях. Действительно, некоммерческий банк крови, который обслуживает и сотрудничает в исследованиях с сотнями больниц, в 2022 году инвестировал нераскрытую сумму в KaloCyte.
Пока что творение Доктора остается в стадии испытаний на животных, но это не единственная попытка упаковать гемоглобин в липиды для создания жизнеспособного заменителя крови. Конкурирующий продукт в Японии уже был испытан на нескольких людях и в целом кажется безопасным.
Однако успех новых продуктов далеко не гарантирован. Всего 2 десятилетия назад более ранние формулы HBOC были отменены или отложены после смерти участников испытаний. Последующие попытки оказались не намного лучше. Самый современный HBOC на сегодняшний день, одобренный для людей в Южной Африке и России, столкнулся с трудностями из-за опасений по поводу побочных эффектов.
Есть веская причина, по которой имитировать кровь трудно — это сложная смесь свободных молекул и клеток. Чуть больше половины крови составляет плазма (желтоватая жидкость, состоящая из воды, белков и солей). Остальное – форменные элементы крови:
- эритроциты (красные кровяные тельца) содержат гемоглобин, который обеспечивает перенос кислорода и придаёт крови красную окраску;
- тромбоциты (кровяные пластинки) обеспечивают свертывание крови после пореза или раны);
- лейкоциты (белые клетки крови) борются с инфекцией.
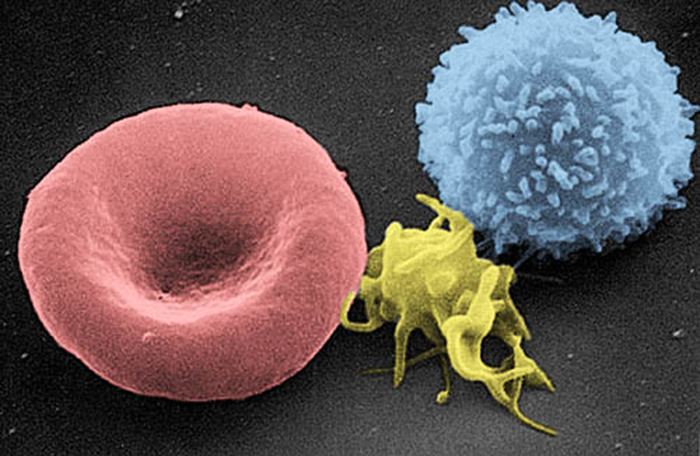
Слева направо: эритроцит, тромбоцит и лейкоцит
Ни одна другая клетка не встречается в большем количестве, чем эритроцит, двояковогнутый диск. Постоянно производимые костным мозгом со скоростью 2 млн/с, эритроциты регенерируют каждые 120 дней. В любой момент времени 30 триллионов клеток совершают забег по 20 000 километров кровеносных сосудов тела.
Проект DARPA также нацелен на разработку синтетических тромбоцитов и лиофилизированной плазмы. Главная цель заключается в том, чтобы имитировать мощный переносчик кислорода. Внутри каждого эритроцита находится приблизительно 260 миллионов молекул гемоглобина. В центре каждого глобулярного белка находится железосодержащий комплекс, называемый гемом. Гемовые комплексы захватывают кислород, становясь ярко-красными и придавая клеткам крови их цвет.
Более ранний класс кандидатов на заменители крови пытался заменить гемоглобин кислородсодержащими химикатами – перфторуглеродами, широко используемыми в хладагентах и огнетушителях. Один из них даже был одобрен Управлением по контролю за продуктами и лекарствами США (FDA) в 1989 году для использования в хирургии. Но сложности изготовления и применения, а также различные побочные эффекты подорвали эффективность продукта, и в конечном итоге он был отозван.
Из-за этого в основном в этой области используются HBOC. Белки гемоглобина внутри эритроцитов соединяются в группы по 4, образуя структуры, называемые тетрамерами. Ранние HBOC часто пытались скопировать такую полимерную конструкцию, но без мембраны. Однако гемоглобин — сложная молекула, токсичная для тканей и сосудов. Во-первых, гемоглобин переносит кислород, который сам по себе является окислителем и может быть разрушительным в неподходящем месте. (Вспомните, как ломтик яблока окисляется и становится коричневым). Нельзя просто впрыснуть гемоглобин в кровоток, как отметил Аллан Доктор.
За последнее столетие у пациентов, получавших заменители крови из незащищенного гемоглобина, развилась гипертония, высокая скорость метаболизма и учащенный пульс. В худших случаях заменители вызывали сердечные приступы и почечную недостаточность, которые, как считалось, были результатом сужения кровеносных сосудов, вызванного свободным гемоглобином. Но были и проблески успеха.
Самым успешным неинкапсулированным HBOC на сегодняшний день является Hemopure, разработанный в 1990-х годах. Он производится путем взятия эритроцитов у коров, извлечения их гемоглобина, очистки его для удаления патогенов и химического связывания четырех белков вместе в виде тетрамера.
Hemopure завоевал раннюю популярность, включая одобрение в Южной Африке в 2001 году — где кризис ВИЧ/СПИД сделал переливание крови высокорискованным методом лечения периоперационной анемии. Однако большая часть использования Hemopure сегодня приходится на ситуации, когда обычные переливания невозможны.
Но перспективы Hemopure изменились в 2008 году, когда The Journal of the American Medical Association (JAMA) опубликовал метаанализ его и четырех других HBOC. Авторы пришли к выводу, что продукты изначально токсичны для сердца, и что пациенты имели на 30% больше шансов умереть, чем при обычном переливании крови.
Испытания были остановлены, инвесторы запаниковали, а компании либо обанкротились, либо полностью прекратили разработку HBOC. Biopure, разработчик Hemopure, был продан через год другой биотехнологической компании.
Первой ошибкой было то, что HBOC назвали заменителем крови. Нет ни одного искусственного продукта, который мог бы сравниться с настоящим. Лучшее, что мы можем сделать, — использовать то, что может временно помочь пациенту, пока костный мозг не сможет вырабатывать больше эритроцитов, как объясняет южноафриканец Заф Зафирелис с почти 80-летним стажем и бывший гендиректор Biopure
«Теперь мы знаем, как можно предотвратить риск, связанный HBOC продуктами, чтобы использовать их для удовлетворения медицинских потребностей», — добавляет Ким Вандегрифф, главный научный сотрудник Vivosang, Inc. Компания разрабатывает собственный HBOC, состоящий из человеческого гемоглобина, связанного с полимер этиленгликоля (полиэтиленгликоль), который часто используется для облегчения доставки лекарств.
Джонатан Уотерс, сотрудник Медицинского центра Питтсбургского университета, использовал Hemopure почти 10 лет для людей, которые отказываются от переливания по религиозным соображениям, или для людей с серповидноклеточной анемией, у которых развиваются реакции на частые переливания крови. Уотерс отмечает, что помнит «10 пациентов, которые умерли бы, если бы им не помог Hemopure».
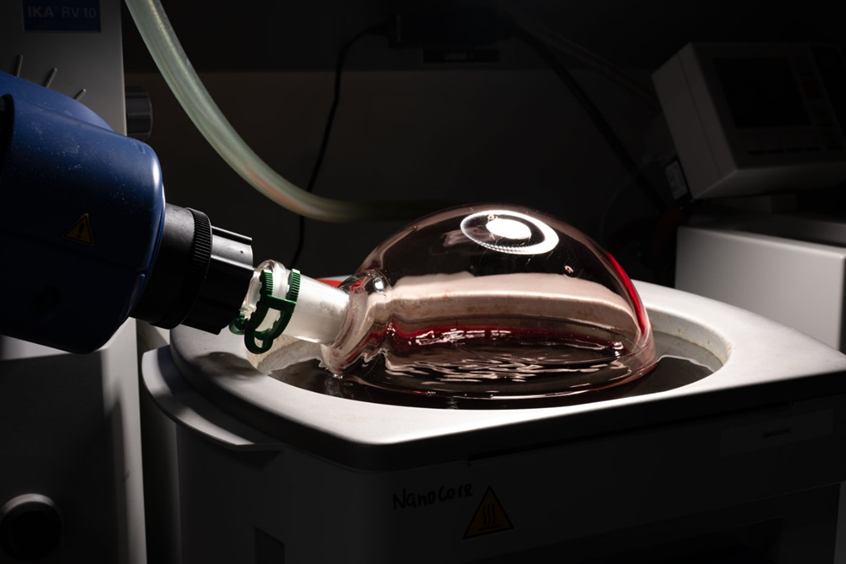
Роторный испаритель помогает извлекать молекулы гемоглобина из донорских эритроцитов, срок годности которых истек. Затем гемоглобин упаковывается в мембраны

Специалист использует фильтровальную машину в чистом помещении, чтобы избавиться от избытка гемоглобина, не инкапсулированного в ErythroMer. Затем жидкость концентрируется в той же машине, получая лиофилизированный продукт

ErythroMer поставляется в лиофилизированном виде. Его текущий срок годности составляет несколько месяцев, но цель KaloCyte – достигнуть срока годности 2 года

Добавление физиологического раствора во флакон с сублимированным ErythroMer создает пригодный для использования синтетический заменитель
В статье Transfusion описан случай, когда врачи не смогли найти подходящую кровь для 54-летней женщины с лейкемией, у которой уровень гемоглобина упал до 2,5 г/дл, что составляет менее 20% от здорового уровня. Врачи ввели женщине 17 единиц (4,25 литра) гемопрофилактики и наблюдали, как уровень гемоглобина стабилизировался до 9,7 г/дл.
В 2014 году Зафирелис основал новую компанию, которая лицензировала технологию, лежащую в основе Hemopure, и пыталась получить полное одобрение FDA. Но все, на что согласилось агентство, — это использование технологии в качестве «нового исследуемого препарата» для пациентов, у которых нет другой альтернативы или которые отказываются от донорской крови. (Почти идентичный родственный продукт, Oxyglobin, одобрен для использования у домашних животных в США и других странах.)
Зафирелис, который сам регулярно отправляет врачам пакеты с гемопротектором Hemopure, по состоянию на май, все еще пытался собрать деньги для пополнения производственных мощностей своей новой компании Hemoglobin Oxygen Therapeutics LLC.
У ErythroMer пока нет клинических историй успеха, но теперь у него есть миллионы, выделенные агентством DARPA. Доктор считает, что он может избежать токсичности чистых продуктов гемоглобина — еще более точно имитируя природу и заключая молекулы в оболочку, как это делают эритроциты.
Доктор никогда не ставил себе целью разработать заменитель крови. В начале 2000-х годов, будучи младшим преподавателем в Университете Вирджинии, Доктор изучал взаимосвязь между гемоглобином и оксидом азота, газом, выделяемым в кровь оболочкой кровеносных сосудов. Сосуды расширяются в присутствии оксида азота и сужаются без него. А эритроциты контролируют его уровень, поскольку, как и кислород, оксид азота может связываться с гемоглобином. Клетки либо изолируют, либо экспортируют оксид азота в зависимости от движения кислорода между ними и тканями в микросреде.
Представьте себе человека, который делает жим лежа. Сначала увеличивается потребление кислорода мышцами, затем увеличивается приток крови, чтобы поддерживать активность тканей, и медленно возвращается к норме после ее прекращения. Поскольку эритроциты доставляют кислород к работающим мышцам, они также выделяют оксид азота, который расширяет региональные кровеносные сосуды, увеличивая местный кровоток. Когда тренировка заканчивается, эритроциты больше не выделяют много кислорода, и их связь с оксидом азота меняется на противоположную — они начинают поглощать газ, который связывается с гемоглобином клетки, и сосуды сужаются.
Имитация клеток крови
Заменители крови из свободного гемоглобина (hemoglobin, Hb) могут быть токсичными. Поэтому некоторые ученые заключают гемоглобин в мембрану, наподобие миниячейки. Например, ErythroMer имеет мембрану, которая улучшает кровоток в сосудах и предотвращает поглощение свободного гемоглобина оксидом азота, газом, который поддерживает кровеносные сосуды открытыми.
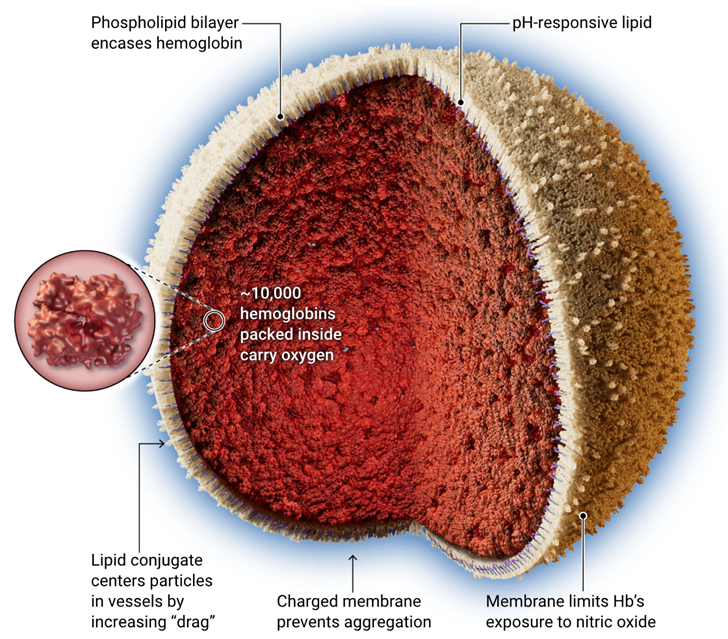
Модель ErythroMer
Вдох-выдох
Как и эритроциты, ErythroMer использует молекулу 2,3-DPG для регулирования сродства гемоглобина к кислороду. В легких 2,3-DPG связывается с синтетической молекулой KC1003, чувствительной к pH, позволяя гемоглобину поглощать кислород. В более кислых тканях 2,3-DPG высвобождается и присоединяется к Hb, способствуя высвобождению кислорода.
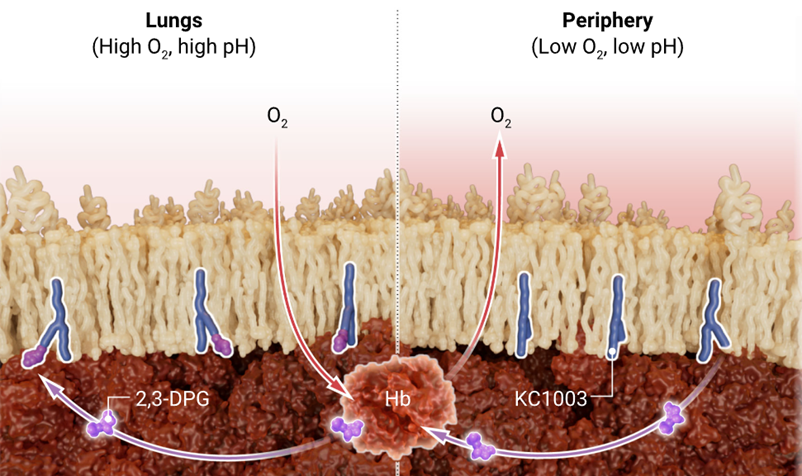
Активность молекулы 2,3-DPG в легких и в более кислых тканях
Сотрудничество во благо
Такая сложная биохимическая хореография преследует мир искусственных переносчиков кислорода, объясняя многие побочные эффекты неинкапсулированных HBOC. Плавая в плазме, свободный гемоглобин может поглощать слишком много оксида азота, вызывая вазоконстрикцию, что может привести к гипертонии и даже сердечному приступу или инсульту. Метаанализ JAMA, опубликованный в 2008 году, выделил такое взаимодействие между гемоглобином и оксидом азота как проблему.
Исследователи предположили, что HBOC, инкапсулирующий гемоглобин, может избежать вазоконстрикции, но никто не знал, как его спроектировать. Однако в 2010 году Дипанджан Пан, инженер-химик Вашингтонского Университета WUSTL, проектировал липидные наночастицы, микроскопические мембраны из жира, для приложений визуализации.
Как позже рассказывал Пан, наночастицы не только напоминали структуру эритроцитов, но и «могли нести очень большое количество гемоглобина». К этому моменту Доктор в том же университете основал лабораторию, изучающую эритроциты при различных заболеваниях и то, насколько хорошо клетки сохраняют свою функцию после хранения. Вскоре Пан и Доктор стали сотрудничать в работе с наночастицами.
«Я знал, что проблемы со старыми HBOC заключались в том, что они были свободны в плазме, и нам нужно было найти способ покрыть гемоглобин. Никто никогда не делал этого на должном уровне», — говорит Доктор.
Ученые объединились и начали разрабатывать искусственные эритроциты. В итоге Пан и Доктор привлекли Филиппа Спинеллу, эксперта по военной трансфузионной медицине в WUSTL. В 2016 году они втроем основали компанию KaloCyte.
Как и его предшественники, ErythroMer содержит гемоглобин, в данном случае собранный из донорских человеческих эритроцитов, срок годности которых истек. Исследовательская группа заключает переработанный гемоглобин в искусственную мембрану, имитирующую то, как эритроцит контролирует захват и высвобождение кислорода.
Если ErythroMer получит широкое распространение, его поставки могут закончиться, но лаборатория Доктора планирует изучить возможность получения гемоглобина в рекомбинантных дрожжах.
Разработанные в первую очередь Паном, мембранные компоненты — всего их пять — включают запатентованный липид под названием KC1003, который команда разработала для реагирования на локальный pH. KC1003 регулирует доступность 2,3-DPG (молекула, встречающаяся в эритроцитах), внутри искусственной мембраны гемоглобина.
Ученые имитировали механизм в эритроцитах для оптимизации доставки кислорода из легких в ткани. Оксид азота все еще может проникать через искусственную мембрану и связываться с гемоглобином внутри, но делает это очень медленно. Основная идея — не мешать передаче сигналов между эритроцитами и кровеносными сосудами. Другими словами, цель — не нарушать нормальные модели вазоконстрикции (сужение) и вазодилатации (расширение) кровеносных сосудов.
ErythroMer все еще находится на ранних стадиях тестирования. Последние доклинические данные продемонстрировали эффективную доставку кислорода мышам, у которых 70% объема крови было заменено ErythroMer. А в случае кроликов вливание жидкости, содержащей ErythroMer, реанимировало животных, как это делает настоящая кровь. Врачи надеются провести первоначальные испытания ErythroMer на здоровых людях, возможно, до истечения гранта DARPA через 4 года.
Продукт KaloCyte – не единственный в мире инкапсулированный гемоглобин. В Японии команда под руководством химика Хироми Сакаи из Медицинского университета Нара сделала нечто подобное, поместив гемоглобин в липидные пузырьки (везикулы гемоглобина, HBV). Везикулы проще ErythroMer, без мембраны, но продукт находится на более высоком уровне разработки.
Испытание безопасности первой фазы на мужчинах HBV было прервано пандемией коронавируса в 2020 году, но первоначальные результаты оказались обнадеживающими. Побочные эффекты включали сыпь и лихорадку, но они были временными, и клинически значимых изменений в жизненных показателях участников не было. То есть, по сравнению с первым поколением HBOC, у HBV меньше шансов (если они вообще есть) вызвать инфаркт миокарда.
Другие инновационные идеи по замене эритроцитов также все еще изучаются. Например, компания Hemarina разрабатывает продукт, который использует свободный гемоглобин, содержащийся в крови морских червей.
Перспективы технологии
Каковы шансы, что какой-либо из новых HBOC станет полноценным заменителем крови? По крайней мере один эксперт, травмированный неудачами в этой области, настроен скептически. Джон Хесс, врач и профессор Вашингтонского университета, заявил, что гемоглобин в оболочке, вероятно, заполнит слишком много места в кровеносном сосуде и не будет переносить достаточно кислорода, чтобы быть полезным.
Отставной полковник армии США, Хесс руководил военной программой разработки продуктов крови с 1991 по 2001 год. Хесс остановил работу над продуктами гемоглобина в 1997 году, потому что не был уверен в безопасности HBOC и не мог найти пути к успешной реализации проекта.
Другие видят больше перспектив. Например, Ким Вандегрифф утверждает, что ученые достаточно близки к пониманию работы заменителей, и при соответствующем финансировании один или несколько из них появятся на рынке. Вандегрифф добавил, что такой продукт остается крайне неудовлетворенной медицинской потребностью.
В конце концов, поскольку врачи разрабатывают новые и улучшенные способы против сильного кровотечения, спрос на экстренный заменитель крови, который долго хранится и подходит всем, только усилился.

